|
| | Dťtermination
de l'aciditť totale d'un jus ou d'un vin ©
Copyright : Marc De Brouwer / CEPvdqa
| Pour en savoir plus
sur l'aciditť des moŻts et des vins et leur dťtermination (cas
particulier des vins rouges), voyez le traitť de
vinification dont sont extraits les principales explications
ci-dessous |
|
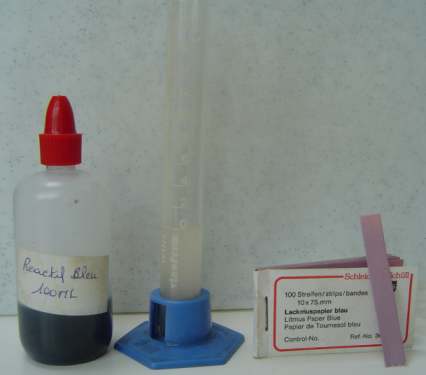
Ci-contre, l'appareillage
nťcessaire ŗ la mesure de l'aciditť totale d'un moŻt ou d'un jus.
(il s'agit ici d'un appareillage simple vendu souvent en kit) :
De gauche ŗ
droite :
-
Liquide rťactif (solution alcaline de couleur bleue due ŗ la prťsence
de bleu de bromothymol
qui prend cette couleur entre pH 6 et 7,6)
-
Eprouvette
spťcialement graduťe,
appelťe ACIDOMETRE
-
Papier Tournesol (papier indicateur)
Utiliser toujours
un liquide aussi limpide que possible, filtrť au papier filtre pour
enlever les matiŤres solides et permettre une lecture aisťe et
prťcise. |
 |
 |
Remplir
l'ťprouvette de jus jusqu'ŗ la graduation 0. Cette quantitť de
liquide correspond trŤs prťcisťment ŗ 10 ml. On peut aussi, en
utilisant une pipette de 10 ml, prťlever exactement 10 ml de liquide ŗ
analyser.
Attention de bien
lire le niveau du liquide, en tenant compte de la tension superficielle
du liquide. La lecture se fait au-dessous du mťnisque (bulle). Chaque
graduation au-dessus du 0 correspond ŗ 1 g díaciditť. La lecture est
directe et facileÖ
Le jus des photos
est un jus de rhubarbe dont líacide oxalique a ťtť neutralisť par líajout
de 2 g de carbonate de calcium par litre. Son aciditť a ainsi chutť de
3 g par rapport ŗ ce quíelle ťtait au dťpart. Líaciditť de
dťpart díun jus de rhubarbe est compris díenviron 14 g (en acide
tartrique), on síattend ŗ ce que la neutralisation se produise dŤs
9/10 g
|
 |
 |
 |
 |
 |
| Complťter,
goutte ŗ goutte, par du rťactif jusqu'ŗ la graduation 6, par exemple. |
Mťlanger intimement le jus et le rťactif en retournant 2 ŗ 3 fois
l'ťprouvette, auparavant on bouche l'orifice ŗ l'aide du pouce.
La couleur ainsi
obtenue sera jaune. |
On ajoutera du rťactif bleu jusqu'ŗ la graduation
suivante : 8,6. |
On mťlange ŗ nouveau. |
Et ainsi de suite, jusqu'ŗ ce que
le mťlange prťsente une couleur vert-bleutť ; dans notre
exemple, il marquera la graduation 9: la solution a rťagi. |
L'amateur peu
expťrimentť et le vinificateur mťticuleux peuvent vťrifier le moment
exact de la neutralisation en ayant recours au papier tournesol.
Le papier
tournesol est vendu sous forme d'une pochette comprenant une trentaine
de bandelettes de couleur bleu mauve. Lorsqu'une bandelette est en
prťsence d'un milieu acide, elle vire au rose.
Si le milieu est
basique (ou alcalin) elle reste mauve. Pour vťrifier si l'aciditť du
vin a ťtť neutralisťe, on prend ŗ l'aide d'une pipette par exemple,
une goutte du vin traitť et on la dťpose sur une bandelette de papier
tournesol.
Si la couleur
vire au rose, il est trop tŰt pour lire sur l'ťprouvette l'aciditť du
vin.
Si la couleur est
plus bleue que mauve, c'est que trop de rťactif bleu a ťtť ajoutť.
Il est ainsi
aisť de dťterminer le moment prťcis de la neutralisation.
Attention : le
papier tournesol rťagit avec l'aciditť de l'air due au gaz carbonique
et devient rose ŗ son contact. Il doit Ítre conservť dans un
emballage ťtanche (boÓte, plastique,...). |
 |
 |
La lecture
de l'aciditť s'effectue en dessous du mťnisque que forme le
liquide avec les bords de l'ťprouvette.
Dans le
cas de la mesure d'une aciditť, le mťnisque est bombť vers le
bas et la lecture se fait par dessous.
La lecture
correcte des photos sera donc de 10,2 (photo de droite - liquide
vu par transparence) et non de 10,4 comme lu ŗ gauche |
 |
| Si vous oubliez
votre ťprouvette quelques heures, ne vous ťtonnez pas de voir la couleur s'ťclaircir.
Cela ne signifie pas que l'analyse effectuťe plus tŰt n'est pas
correcte. Ce phťnomŤne est dŻ au fait qu'un nouvel ťquilibre
chimique se produit dans le liquide contenu dans l'ťprouvette: certains
acides se dissocient de leurs sels... |
|
Labo Vin
est un site proposant un programme gratuit, utilisable en ligne ŗ
ceux dont la profession ou le hobby est de fabriquer des vins,
vins de fruits, liqueurs... Il leur facilitera le travail en
calculant pour eux rapidement et sans erreur tous les paramŤtres
qui interviennent dans cette activitť : concentrations et
volumes de sucre, d'alcool, mesures d'aciditť, de densitť... |
|
|












